2023年10月11日�����,為規范醫療器械人因設計注冊申報資料和審評要求���,器審中心組織起草了《醫療器械人因設計注冊審查指導原則(征求意見稿)》���,即日起第二次公開征求意見���。醫療器械人因設計及可用性工程,醫療器械注冊檢驗需要提交的醫療器械可用性工程文檔即是此要求之一���。詳見正文。
2023年10月11日��,為規范醫療器械人因設計注冊申報資料和審評要求����,器審中心組織起草了《醫療器械人因設計注冊審查指導原則(征求意見稿)》�,即日起第二次公開征求意見。詳見正文�����。
醫療器械人因設計注冊審查指導原則(第二次公開征求意見稿)
本指導原則旨在指導注冊申請人建立醫療器械人因設計過程和準備醫療器械人因設計注冊申報資料,同時規范醫療器械人因設計技術審評要求��。
本指導原則是對醫療器械人因設計的一般要求。注冊申請人需依據產品具體特性和風險程度確定本指導原則具體內容的適用性���,若不適用詳述理由。注冊申請人也可采用其他滿足法規要求的替代方法���,但需提供詳盡的支持資料���。
本指導原則是在現行法規���、強制性標準體系以及當前科技能力、認知水平下制定的,隨著法規、強制性標準體系的不斷完善以及科技能力����、認知水平的不斷發展,本指導原則相關內容也將適時調整。
本指導原則是供注冊申請人����、審評人員和檢查人員使用的指導文件,不涉及行政審批事項,亦不作為法規強制執行���,應在遵循相關法規的前提下使用本指導原則���。
本指導原則是醫療器械人因設計的通用指導原則��,其他醫療器械指導原則可在本指導原則基礎上結合具體情況進行有針對性的調整���、修改和完善����。
一、適用范圍
本指導原則適用于第二類��、第三類醫療器械人因設計的注冊申報����,不適用于體外診斷試劑����。醫療器械注冊申請人可參照本指導原則要求開展全部醫療器械的人因設計工作���。
二����、主要概念
(一)人因設計和可用性
從醫療器械安全有效性評價角度出發���,本指導原則所述人因設計是指綜合運用關于人類的解剖、生理����、心理�、行為�����、文化等方面能力與限制的人因工程知識來設計開發醫療器械�����,以增強醫療器械的可用性�����。人因工程亦稱可用性工程����、人機工效學/人體工程學�,人因工程知識包括但不限于身體�、感知��、認知��、行動等方面知識。
可用性(Usability)是指預期用戶在預期使用場景下正常使用醫療器械時,保證醫療器械安全有效使用的用戶接口易用特性。易用特性包括但不限于易讀性�、易理解性、易學習性�����、易記憶性���、易操作性、用戶差錯防御性等特性��。本指導原則所述可用性僅限于與醫療器械安全有效使用相關的用戶接口特性���,注冊申請人可參考本指導原則設計開發其他用戶接口特性�,如用戶滿意度����、使用意愿等�����。
(二)用戶����、使用場景和用戶接口
用戶�����、使用場景和用戶接口是人因設計的三個核心要素��。
1.用戶
用戶是指注冊申請人所規定的醫療器械操作人員,如醫務�、患者���、家庭護理、清潔���、運輸����、安裝�、維修��、處置等人員����。用戶通?��?煞譃槎鄠€用戶組����,用戶組即具有某一用戶特征的用戶人群�����。用戶特征用于反映用戶組自身在解剖��、生理����、心理�����、行為�、文化等方面的獨特性,包括但不限于用戶人群的人口統計學(如性別、年齡)��、人體測量學(如身高、體重、力量)����、能力(如感知��、認知�、行動)、文化(如社會關系、職業傳統、語言)等方面特征以及知識水平�、職業技能、工作經驗��、培訓程度等方面要求�。
用戶若為或含有兒童�、老人���、孕婦以及殘障人士等特殊人群�,由于其用戶特征與普通人群存在較大差異�����,故需考慮可及性要求�。同時��,亦需綜合考慮用戶在健康����、疾病�、服藥等不同狀態下的能力及其限制����,必要時明確用戶限制�。
注冊申請人需根據醫療器械用戶特征情況規定用戶/用戶組要求���。本指導原則重點關注醫務、患者�、家庭護理等操作醫療器械實現其預期用途的用戶/用戶組�����,包括醫療器械消毒滅菌操作人員,暫不考慮清潔���、運輸�����、安裝���、維修�����、處置等操作人員�,待時機成熟時納入考量。不過注冊申請人需考慮全部用戶/用戶組的人因設計要求����。
2.使用場景
如圖1所示,使用場景是指注冊申請人所規定的醫療器械實際使用的場景因素��,包括使用環境和操作任務�。使用環境是指用戶操作醫療器械的實際環境�����,又可分為使用場所、環境條件,其中使用場所包括門診室、急診室、手術室�、病房、救護車���、家庭、公共場所等情況,環境條件包括空間���、照明、溫度、濕度、氣壓��、潔凈度、噪聲���、振動�、輻射等情況�����。操作任務是指用戶操作醫療器械以實現特定目標的行動或行動序列���,本指導原則重點關注醫療活動相關操作任務�,暫不考慮清潔��、運輸����、安裝�、維修、處置等操作任務(醫療器械安全標準若有相應要求除外),待時機成熟時納入考量。不過注冊申請人需考慮全部操作任務的人因設計要求��。
操作任務從不同角度出發有不同分類方法。從風險角度可分為關鍵任務和非關鍵任務�,關鍵任務是指用戶行動或行動缺失可能導致嚴重傷害或死亡的操作任務��,反之即為非關鍵任務���。從操作緊迫性角度可分為緊急任務和非緊急任務�,緊急任務是指需要用戶立刻執行的操作任務,反之即為非緊急任務����。從操作頻率角度可分為常用任務和非常用任務�����,常用任務是指用戶經常使用的操作任務���,反之即為非常用任務。關鍵任務�����、緊急任務和常用任務相互關系如下:緊急任務通常屬于關鍵任務��,常用任務與關鍵任務、緊急任務存在交集��,某一特定操作任務可以同時為上述二種或三種任務。本指導原則關注醫療器械潛在使用風險��,故以關鍵任務作為操作任務分類主線�,兼顧緊急任務和常用任務,即重點關注兼為緊急任務���、常用任務的關鍵任務���。
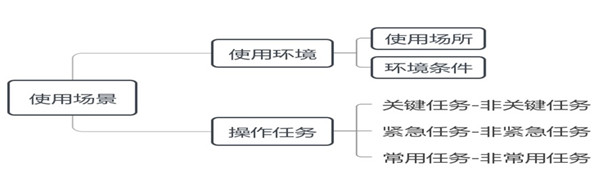
圖1:使用場景
注冊申請人需規定醫療器械關于使用場所���、環境條件和操作任務的要求,并識別關鍵任務及其風險,特別是兼為緊急任務、常用任務的關鍵任務。
3.用戶接口
用戶接口(又稱用戶界面)是指用戶與醫療器械人機交互的全部對象及方式,包括醫療器械的形狀尺寸重量��、顯示反饋���、連接組裝、操作控制�、說明書與標簽���、包裝�、用戶培訓材料等��。
注冊申請人需以操作任務為導向,結合用戶��、使用場所��、環境條件進行用戶接口設計���。
(三)醫療器械使用情況和用戶操作情形
1.醫療器械使用情況
如圖2所示,醫療器械使用情況可分為正常使用和非正常使用���,其中正常使用是指用戶按照說明書要求及常識慣例操作醫療器械����,反之即為非正常使用。
正常使用從使用結果角度可分為正確使用和錯誤使用����,其中正確使用是指沒有錯誤使用的正常使用�����,其產生的風險均可接受;錯誤使用是指用戶行動或行動缺失導致異于注冊申請人或用戶所預期的醫療器械響應,其可能降低醫療器械的有效性或者產生不可接受的風險,導致患者���、用戶或相關人員受到傷害或死亡���。
使用錯誤是指可能導致錯誤使用的潛在根源�����,可分為感知錯誤�、認知錯誤和行動錯誤����。其中��,感知錯誤是指用戶對視覺、聽覺�、觸覺等信息感知失效所致的使用錯誤,如看錯輸出結果單位���、未聽到報警聲音等�����;認知錯誤是指用戶對知識�����、規則�����、信息存在記憶、理解等認知失效所致的使用錯誤��,如漏記手術操作步驟��、誤解符號含義等;行動錯誤是指用戶操作失誤�、不當等行動失效所致的使用錯誤�,如按錯控制按鈕、按壓力度不夠而未激活等�����。
非正常使用包括非預期用戶使用�����、用戶故意違背要求使用或二者兼而有之等情況���,其中非預期用戶使用可分為可合理預見��、非可合理預見兩種情況�����。
雖然注冊申請人可參考本指導原則識別醫療器械非正常使用的風險,但本指導原則僅限于醫療器械正常使用的風險考量�,同時從風險管理角度考慮可合理預見非預期用戶使用的風險��,如供成人使用的家用醫療器械需考慮兒童使用風險。
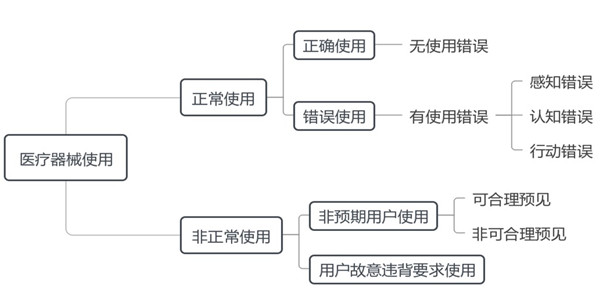
圖2:醫療器械使用情況
2.用戶操作情形
如圖3所示����,用戶實際使用醫療器械的操作情形較為復雜,本指導原則根據操作任務完成程度將其分為操作成功��、操作困難����、操作險肇����、操作失敗。
操作成功是指滿足期望的操作任務完成,屬于預期的正確使用。操作困難是指低于期望但符合要求的操作任務完成�����,如操作時間較長或效率較低��,亦含僥幸完成操作任務���,屬于非預期的正確使用,即使用困難,需要根據具體情況加以改進��。操作險肇[1]是指幾乎出現不可接受風險的操作任務完成,如用戶未按使用警示操作,但及時采取糾正措施使得沒有發生錯誤使用��,或者及時采取補救措施使得錯誤使用沒有導致傷害,是操作困難的特殊情形,屬于非預期的正確使用,即使用險肇(Close call)����,需要采取預防措施以控制潛在使用風險����。操作失敗是指不滿足期望的操作任務完成或者未能完成操作任務,包括操作超時����、操作失誤、操作省略、操作中止等情形��,這些情形可能同時發生���,均屬于錯誤使用��,需要采取糾正措施以降低使用風險�����。因此�,醫療器械實際使用情況可細分為正確使用、使用困難、使用險肇��、錯誤使用����。
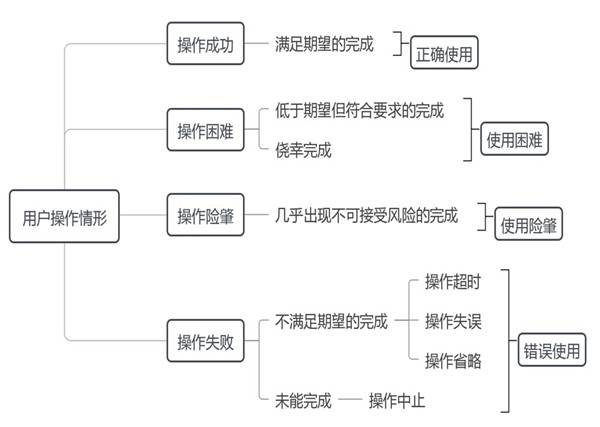
圖3:用戶操作情形
注冊申請人需基于醫療器械實際使用情況��,結合用戶和使用場景,采取相應措施加強用戶接口設計�,保證醫療器械使用的安全有效性�。
三�、基本原則
(一)人因設計定位
醫療器械在使用階段需要人機交互方能實現其預期用途,人機交互核心問題在于用戶接口設計能否保證醫療器械使用的安全有效性�。因此本指導原則聚焦于醫療器械的用戶接口設計問題��,從醫療器械設計開發角度考慮人因設計相關要求。
醫療器械人因設計是醫療器械安全有效性的重要組成部分,需基于醫療器械的預期用途�、使用場景���、核心功能分析并控制醫療器械使用風險����,結合用戶和使用場景開展用戶接口設計��,不能脫離安全有效性孤立進行人因設計�。
(二)使用風險導向
醫療器械人因設計若存在問題將不利于人機交互��,可能產生使用風險,影響到醫療器械使用的安全有效性�����。同時��,醫療器械不良事件和召回數據也表明醫療器械使用問題較為突出���,使用風險不容忽視�,主要原因在于醫療器械人因設計存在問題。因此��,醫療器械需要加強人因設計,特別是在采用全新使用方式���、學習曲線長、非專業用戶使用����、生命支持、藥械聯用、急救��、家用、適用于脆弱人群(如兒童��、孕婦���、老人)等情況下���。
考慮到使用風險所致傷害發生概率在執行層面難以統計�����,故將醫療器械使用風險按傷害嚴重度分為高�、中、低三個級別���,分別指錯誤使用可能導致嚴重傷害或死亡、可能導致輕微傷害���、不可能導致傷害。根據關鍵任務的定義�,高使用風險醫療器械含有關鍵任務,中��、低使用風險醫療器械不含關鍵任務���。
醫療器械使用風險級別可通過風險管理進行判定����,原因在于醫療器械使用風險是醫療器械風險管理的重要組成部分�����。風險管理所定義的風險等級與本指導原則所述醫療器械使用風險級別可以不同����,不過二者存在對應關系�����,因此可根據風險管理所定義的風險等級來判定醫療器械使用風險級別�����,但需在采取風險控制措施之前進行判定。
值得注意的是,高使用風險醫療器械屬于高風險醫療器械(可能導致嚴重傷害或死亡的醫療器械)��,但高風險醫療器械并非都是高使用風險醫療器械����,若其采用全新使用方式����、學習曲線長、非專業用戶使用通常屬于高使用風險醫療器械,即高風險醫療器械若含有關鍵任務則為高使用風險醫療器械。
同時���,醫療器械使用風險級別還可通過同類醫療器械上市后不良事件和召回情況進行判定,即同類醫療器械上市后發生與用戶使用和/或用戶接口設計相關的嚴重不良事件或一級召回屬于高使用風險,發生不良事件或二級召回屬于中度使用風險���,未發生不良事件且僅發生三級召回或無召回屬于低使用風險�����。
醫療器械人因設計需結合用戶、使用場景和用戶接口開展風險管理�,采用失效模式與效應分析(FMEA)�、故障樹分析(FTA)等風險分析方法及其衍生方法�����,通過用戶接口設計(首選)����、防護措施、安全信息等風險控制措施將醫療器械使用風險降至可接受水平,必要時開展用戶培訓����,特別是對高使用風險醫療器械�����。
考慮到行業實際情況,高使用風險醫療器械當前僅限于部分第三類醫療器械,詳見附件1�;未在醫療器械分類目錄的全新第三類產品可根據上述方法判定其使用風險級別����。
(三)全生命周期管理
醫療器械全生命周期均需考慮人因設計要求�。上市前將人因設計納入醫療器械設計開發和風險管理過程,識別可預見的使用風險并將其降至可接受水平��。上市后結合醫療器械使用問題(含不良事件和召回�,下同)���,識別前期未預見的使用風險并改進人因設計,進一步提高醫療器械使用的安全有效性�����。
醫療器械人因設計是一個反復迭代、逐步細化的過程���,注冊申請人需在質量管理體系設計開發程序的框架下開展人因設計可追溯性分析,即識別���、追蹤并分析人因設計的輸入��、輸出�、驗證�、確認、風險管理之間的關系�����,人因設計更改亦需開展人因設計可追溯性分析���。
綜合考慮行業發展水平和使用風險分級管理導向�,醫療器械使用風險級別不同���,其人因設計的生命周期質控要求和注冊申報資料要求亦不同��。注冊申請人需基于風險管理��,結合同類醫療器械上市后不良事件和召回情況,依據風險從高原則綜合判定醫療器械使用風險級別�����,并采取與之相適應的生命周期質控措施:高使用風險醫療器械原則上需開展完整人因設計生命周期質控工作,中���、低使用風險醫療器械可基于風險管理過程開展人因設計生命周期質控工作。高使用風險和中����、低使用風險醫療器械注冊申報資料的差異詳見第八章�。
四、人因設計過程
醫療器械人因設計是醫療器械設計開發的重要組成部分��,注冊申請人需在質量管理體系設計開發過程的框架下建立充分��、適宜�����、有效的人因設計過程。人因設計過程包括用戶接口的需求分析���、設計、實現��、驗證����、確認���、更改等活動�����,風險管理和可追溯性分析貫穿于其中�����,且每個活動均需形成相應人因設計文檔。
人因設計的需求分析活動是指從用戶接口概念定義到形成用戶接口需求規范的全部活動?���;谟脩艚涌谛枨笳{研�����、前代醫療器械用戶接口設計以及同類(含前代,下同)醫療器械上市后使用問題等情況,明確醫療器械的預期用途���、適用人群���、用戶組���、用戶特征�����、使用場所、環境條件��、人機交互方式、操作任務�,識別關鍵任務并開展風險分析,確定用戶接口的技術特征及其使用錯誤��,形成用戶接口需求規范�。根據用戶接口需求規范建立用戶接口確認計劃���。可追溯性分析此時追溯用戶接口需求與產品需求�、用戶接口需求與風險分析的關系���。
人因設計的設計活動是指從用戶接口需求規范到形成用戶接口設計規范的全部活動?����;谟脩艚涌谛枨笠幏洞_定用戶接口技術特征的實現方案以及使用錯誤的風險控制措施,包括說明書與標簽�����、用戶培訓材料��,形成用戶接口設計規范���。根據用戶接口設計規范建立用戶接口驗證計劃��?����?勺匪菪苑治龃藭r追溯用戶接口設計與用戶接口需求、用戶接口設計與風險控制的關系����。
人因設計的實現活動是指基于用戶接口設計規范實現用戶接口的全部活動,包括說明書與標簽����、用戶培訓材料。人因設計實現活動需結合風險管理予以實施����。
人因設計的驗證活動是確保用戶接口符合用戶接口設計規范的全部活動�。人因設計驗證活動基于用戶接口驗證計劃形成用戶接口驗證報告�����?��?勺匪菪苑治龃藭r追溯用戶接口驗證與用戶接口設計�����、用戶接口驗證與風險管理的關系���。人因設計驗證具體要求詳見第五章����。
人因設計的確認活動是確保用戶接口滿足用戶需求的全部活動�。人因設計確認活動基于用戶接口確認計劃形成用戶接口確認報告����,并確保綜合剩余使用風險均可接受。可追溯性分析此時追溯用戶接口確認與用戶接口需求����、用戶接口確認與風險管理的關系�。人因設計確認具體要求詳見第五章��。
人因設計的更改活動包括用戶接口更改請求評估�����、更改策劃���、更改實施��、驗證����、確認、風險管理����、可追溯性分析、文檔控制等活動。
醫療器械人因設計過程可根據醫療器械相關設計開發活動的具體情況選擇適宜的人因工程方法及其組合����,人因設計常用方法詳見附件2,人因設計基本要素詳見附件3。
五��、人因設計驗證與確認
人因設計驗證與確認是醫療器械設計驗證與確認的重要組成部分,即人因設計驗證屬于設計驗證,人因設計確認屬于設計確認�。從人因工程角度出發��,人因設計驗證又稱為形成性評價,包括從用戶接口概念定義到用戶接口設計基本定型的全部質量保證活動,是人因設計確認的基礎。人因設計確認又稱為總結性評價,用于確保已設計定型的用戶接口滿足用戶需求,且綜合剩余使用風險均可接受����。
若適用�����,人因設計驗證與確認需涵蓋特殊用戶人群和特殊使用環境。
(一)形成性評價
形成性評價可采用或組合采用專家評審���、認知走查���、形成性可用性測試等方法。
形成性可用性測試即人因設計驗證測試,注冊申請人可采用模擬測試(基于模擬使用場景、基于自建可用性實驗室)��、對比測試(基于已上市同類醫療器械)等方法,也可委托第三方可用性實驗室(含檢測機構���、高校����、研究機構等)開展模擬測試���。
形成性可用性測試的參與人員數量根據相關研究結果�,通常設定為每個用戶組5至8人,能夠發現多數使用錯誤�����?����?砷_展多次形成性可用性測試,每次可選擇不同可用性測試方法�,并可根據具體情況確定測試參與人員數量。
形成性可用性測試需制定測試計劃�,依據測試計劃開展測試�����,并形成測試報告��。需考慮測試的目的、參與人員��、對象、方法��、任務�、實施���、數據收集��、結果分析等要求���,根據測試所發現的使用錯誤�����、使用困難、使用險肇���,結合風險管理采取相應風險控制措施改進用戶接口設計����。
(二)總結性評價
總結性評價可采用或組合采用總結性可用性測試��、等效醫療器械對比評價等方式。原則上���,全新產品(無產品上市或安全有效性尚未在醫療實踐中得到充分證實)采用總結性可用性測試方式,成熟產品(安全有效性已在醫療實踐中得到充分證實)可采用等效醫療器械對比評價方式���。
1.總結性可用性測試
總結性可用性測試即人因設計確認測試�,注冊申請人可采用模擬測試(基于模擬使用場景、基于自建可用性實驗室)、現場測試(基于真實使用場景)等方法����,也可委托第三方可用性實驗室(含檢測機構��、高校��、研究機構等)開展模擬測試���。
總結性可用性測試的參與人員數量需統計計算�����,相關研究結果表明15人����、20人�����、30人可分別發現至少90%��、95%、97%的使用錯誤。因此�,總結性可用性測試每個用戶組的測試參與人員數量不少于15人��。
總結性可用性測試基于人因設計定位�,確保測試參與人員均為預期用戶且涵蓋全部關鍵任務涉及的用戶組��,用戶接口已設計定型����,測試環境與真實使用環境相同或等同,全部關鍵任務均已納入����。
總結性可用性測試需考慮測試參與人員的背景���,利益相關人員不得作為測試的參與人員、分析與評估人員,即注冊申請人的產品設計開發人員不能作為模擬測試��、現場測試的參與人員、分析與評估人員,注冊申請人及其利益相關方的員工不能作為模擬測試的參與人員、分析與評估人員��。
為保證受試者安全,現場測試可能無法納入全部關鍵任務,需考慮關鍵任務的測試選擇以及未測關鍵任務補充測試的方法和要求��,并予以記錄��;建議考慮測試參與機構地域分布的多樣性和代表性。
總結性可用性測試過程通常包括測試計劃制定、測試參與人員招募與培訓��、測試實施�����、測試數據收集�、測試結果分析����、測試報告撰寫等活動���。
測試計劃以關鍵任務為導向���,特別是兼為緊急任務�、常用任務的關鍵任務����,明確測試通過/失敗準則���,涵蓋說明書與標簽�、用戶培訓材料測試要求。
測試參與人員招募需考慮人員入排問題�,根據用戶/用戶組的用戶特征選擇測試參與人員�,經常參加同類醫療器械或同一注冊人所屬醫療器械可用性測試的參與人員原則上予以排除。測試參與人員培訓需基于醫療器械產品特性考慮培訓的內容和要求��,特別是學習曲線長的醫療器械可能需要開展多次培訓;若無需開展測試參與人員培訓則需說明原因并予以記錄���。
測試數據包括觀測數據、訪談數據���。其中�����,觀測數據源自測試參與人員操作行為的記錄(含圖片���、視頻等)���,可基于測試參與人員隱私保護考慮對相關記錄進行適當處理�,但需保證操作行為記錄的完整性;訪談數據源自測試參與人員關于產品操作���、使用知識的問答記錄��,問答需包含開放式問題�。使用知識需特別關注知識任務,如說明書與標簽的使用警示�,其無法通過觀測方式予以評價����,故采用訪談方式���。
測試報告包括但不限于測試目的�、測試參與人員�、測試對象�����、測試方法���、測試任務���、測試結果分析��、測試計劃偏離�、結論等內容。其中,測試參與人員明確人員的數量和背景,測試對象提供產品基本信息和實物圖片���,測試方法列明測試所用設備和軟件工具�����,測試任務明確測試的項目、流程����、結果并提供測試圖片��,測試結果分析結合測試數據分類描述每個使用錯誤、使用困難、使用險肇的發生頻率�、潛在傷害�����、使用錯誤類型(感知錯誤�����、認知錯誤���、行動錯誤)及危險源�、風險控制措施、綜合剩余風險��。
總結性可用性測試若測試結果不符合測試通過準則要求���,則需分析并確定測試失敗的原因及其影響���,考慮重新開展總結性可用性測試的范圍和內容���,并予以記錄���。若總結性可用性測試出現風險不可接受的使用錯誤��,則需針對上述使用錯誤實施人因設計更改活動����,并開展補充性總結性可用性測試或者重新開展總結性可用性測試,此時需考慮測試參與人員的選擇問題。
2.等效醫療器械對比評價
本指導原則所述等效醫療器械是指與申報醫療器械在預期用途�、適用人群�、用戶組�����、用戶特征、使用場所����、環境條件�����、關鍵任務���、人機交互方式��、用戶培訓等方面基本等同且已在境內注冊上市的同類醫療器械����。
等效醫療器械對比評價可參考同品種對比臨床評價方式予以開展。首先結合上述判定要素選定申報醫療器械的等效醫療器械�,然后基于上述判定要素逐項進行對比�。若二者無差異��,結合全球主要醫療器械不良事件�����、召回數據庫和國內外文獻綜述開展同類醫療器械上市后使用問題分析,若無新增使用風險采用等效醫療器械在境內注冊上市所用的總結性評價資料作為支持證據�;若有新增使用風險�����,除以上工作外還需開展申報醫療器械針對新增使用風險的總結性評價資料�。
若二者有差異,開展同類醫療器械上市后使用問題分析,若無新增使用風險采用等效醫療器械在境內注冊上市所用的總結性評價資料作為支持證據�����,并提交申報醫療器械針對差異的總結性評價資料;若有新增使用風險,除以上工作外還需開展申報醫療器械針對新增使用風險的總結性評價資料�����。
等效醫療器械對比評價需形成報告�����,包括但不限于評價的目的�、對象��、路徑�、支持證據���、結論以及評價人員簡歷等內容��。其中�,評價對象提供產品基本信息和實物圖片����,評價路徑包括等效醫療器械對比分析、同類醫療器械上市后使用問題分析�,支持證據詳見表1�,評價人員需具備人因設計相關知識和工作經驗���,建議優先考慮醫療器械人因設計專業人士。
表1:等效醫療器械對比評價支持證據
差異性 | 無新增使用風險 | 有新增使用風險 |
申報醫療器械與等效醫療器械無差異 | 1.1等效醫療器械總結性評價資料 2.1同類醫療器械上市后使用問題分析報告 | 1.1等效醫療器械總結性評價資料 2.1同類醫療器械上市后使用問題分析報告 2.2申報醫療器械針對新增使用風險的總結性評價資料 |
申報醫療器械與等效醫療器械有差異 | 1.1等效醫療器械總結性評價資料 1.2申報醫療器械針對差異的總結性評價資料 2.1同類醫療器械上市后使用問題分析報告 | 1.1等效醫療器械總結性評價資料 1.2申報醫療器械針對差異的總結性評價資料 2.1同類醫療器械上市后使用問題分析報告 2.2申報醫療器械針對新增使用風險的總結性評價資料(可與1.2合并) |
等效醫療器械總結性評價資料若因法規前期未作要求而無法提供,則可提供等效醫療器械上市后使用問題分析報告,并可與其同類醫療器械上市后使用問題分析報告合并
。同類醫療器械上市后使用問題分析報告需考慮檢索的范圍���、時效性和個案情況等問題。檢索范圍參照同品種對比臨床評價相應要求,但需考慮不良事件和召回分級的國家差異�;檢索時效性根據同類醫療器械上市時間和產品特性予以考慮��,一般為近十年;個案情況可予以排除�����,但需提供詳實的數據分析����。
若無等效醫療器械��、等效醫療器械對比評價無法開展或證據不足,則需采用總結性可用性測試方式進行總結性評價。
六��、技術考量
(一)臨床試驗
考慮到臨床試驗受試者權益保護要求,人因設計確認測試(即總結性可用性測試)某些關鍵任務測試項目可能會導致受試者受到嚴重傷害或死亡,不能在臨床試驗中予以執行���。同時,人因設計確認測試對于測試參與人員數量有明確要求,臨床試驗參與人員數量不一定能夠滿足相應要求。因此��,臨床試驗通常情況下不能完全替代人因設計確認測試���,但可作為人因設計確認測試的支持和補充�。
在特殊情況下�,臨床試驗可用作人因設計確認測試。高使用風險醫療器械關鍵任務的風險均已采取控制措施降至可接受水平�����,中���、低使用風險醫療器械無關鍵任務,相應臨床試驗若能保證參與人員數量達到要求則可用作人因設計確認測試��。
注冊申請人可根據自身質量管理體系設計開發程序要求,確定人因設計確認測試與臨床試驗的時序關系和評價側重�����。
(二)進口醫療器械
考慮到進口醫療器械在用戶和使用場景方面均存在中外差異�,原有用戶接口設計未必能夠保證醫療器械在中國使用的安全有效性,同時需要考慮中外人因設計注冊申報要求的差異�����,包括用戶范圍���、操作任務范圍���、關鍵任務類型���、總結性可用性測試參與人員數量等方面。因此��,進口醫療器械原則上需基于使用風險級別在中國開展相應人因設計確認工作,除非提供數據詳實的支持材料證實中外差異對于人因設計確認無顯著影響���。
對于高使用風險醫療器械,注冊申請人需結合用戶���、使用場景和注冊申報要求開展中外人因設計差異分析����,若中外差異對于人因設計確認影響的風險可接受,則在人因設計研究報告(詳見第七章)驗證與確認部分提交境外上市總結性評價資料���、同類醫療器械上市后使用問題分析報告、中外人因設計差異分析報告�����。反之�,若中外差異對于人因設計確認影響的風險不可接受,則仍需在中國(或基于中國的用戶��、使用場景和注冊申報要求)開展針對中外差異或者完整的人因設計再確認工作���,并在人因設計研究報告驗證與確認部分提交境外上市總結性評價資料、同類醫療器械上市后使用問題分析報告��、中外人因設計差異分析報告以及相應人因設計再確認資料�����。
對于中����、低使用風險醫療器械��,注冊申請人提交使用錯誤評估報告(詳見第七章)���、境外上市總結性評價資料即可����。
(三)現成用戶接口
現成用戶接口是指注冊申請人未進行(含無法證明)完整人因設計生命周期控制的用戶接口�。使用現成用戶接口需在醫療器械人因設計過程中明確質控要求��,結合其全球上市后使用問題考慮需求分析�、驗證�、確認、風險管理��、可追溯性分析等活動要求�,并在人因設計文檔中予以記錄,以備體系核查或注冊使用���。
醫療器械可使用多個現成用戶接口,需在確認每個現成用戶接口安全有效性的基礎上,從醫療器械產品整體角度確認全部用戶接口(含自研用戶接口��、現成用戶接口)的安全有效性。此時,每個現成用戶接口的安全有效性可參照等效醫療器械對比評價方式進行確認�,重點分析現成用戶接口的上市后使用問題�����。
注冊申請人可全部使用現成用戶接口,亦可部分使用現成用戶接口,即自研用戶接口與現成用戶接口相結合,此時自研部分參照自研用戶接口要求���,現成部分參照現成用戶接口要求����。
(四)組合使用
對于組合使用�,即有源主機與有源附件�、有源設備與無源耗材���、有源設備與試劑盒聯合使用方能實現預期目的���,注冊申請人需從醫療器械系統層面整體進行人因設計確認�,在各自注冊單元中提交醫療器械系統的人因設計研究資料。
(五)標準
注冊申請人可根據人因工程、可用性工程����、人機工效學/人體工程學、職業安全相關國際、國家和行業標準進行醫療器械人因設計���,相關標準可分為過程標準、產品標準、安全標準和基礎標準�。
可依據相應過程標準規范醫療器械人因設計過程���,并根據醫療器械設計開發具體情況選擇適宜的人因設計方法及其組合�。有些醫療器械產品標準已含有用戶接口要求,如連接��、控制等����,可參考相應產品標準的適用要求進行醫療器械人因設計。有些醫療器械安全標準也含有人因設計要求����,如報警����、家庭護理環境�����、緊急醫療服務環境、生理閉環控制等并列安全標準和呼麻類設備����、監護類設備等專用安全標準�,需考慮相應安全標準的適用性。此外�,亦可參考符號�、標識等基礎標準進行醫療器械人因設計。
(六)人因設計更改
醫療器械人因設計更改需按照質量管理體系要求���,開展與之相適應的驗證與確認活動,同時評估其對醫療器械安全有效性的影響�。
醫療器械的用戶��、使用場景����、用戶接口發生實質性更改通常會涉及醫療器械適用范圍����、結構組成�、產品技術要求等注冊證載明事項的一項或多項變更�����,應申請變更注冊����。若未發生實質性更改�����,通過質量管理體系進行控制����,同時形成相應評估文檔���,包含人因設計更改情況���、使用風險管理情況等內容�����,以備體系核查或變更注冊使用����。
醫療器械人因設計更改若涉及使用風險級別的更改����,則需按照更改后的使用風險級別提供相應人因設計注冊申報資料。
七�、人因設計研究資料
(一)人因設計研究報告
人因設計研究報告適用于高��、中�����、低使用風險醫療器械,包括基本信息���、使用風險級別、核心要素、人因設計過程��、需求規范����、使用風險管理、驗證與確認、可追溯性分析、結論等內容����。
1.基本信息
明確申報醫療器械的名稱��、型號規格、預期用途、適用人群�。
2.使用風險級別
明確申報醫療器械的使用風險級別(高�、中、低),并詳述判定理由(詳見第三章)�。
3.核心要素
明確申報醫療器械的用戶��、使用場景、用戶接口�。其中�,用戶詳述用戶組設置情況及相應用戶特征。使用場景在詳述使用場所���、環境條件的基礎上,重點闡述關鍵任務(若兼為緊急任務���、常用任務需注明)的操作序列����、預期結果��。用戶接口詳述人機交互方式,提供用戶接口圖示及注釋�。
若有多個型號規格��,詳述在核心要素方面的差異,并開展差異影響評估��。
4.人因設計過程
提供申報醫療器械的人因設計過程流程圖,并依據流程圖詳述人因設計過程各個活動的內容和要求�����,提供人因設計文檔(可用性工程文檔)索引表�����。
若有,可提供人因設計相關過程標準核查表�,用于替代相應描述����。
5.需求規范
提供申報醫療器械的用戶接口需求規范文檔,若無單獨的用戶接口需求規范文檔���,可提供產品需求規范文檔并注明用戶接口需求所在位置。
6.使用風險管理
提供申報醫療器械采取風險控制措施前后的使用風險矩陣匯總表�����,以及使用風險管理文檔��。若無單獨的使用風險管理文檔���,可提供產品風險管理文檔并注明使用風險所在位置��。
使用風險管理文檔需結合同類醫療器械上市后使用問題的分析,涵蓋申報醫療器械全部已知使用錯誤的風險分析及其風險控制措施����,確保綜合剩余使用風險均可接受����。
7.驗證與確認
述申報醫療器械人因設計驗證與確認(即形成性評價和總結性評價)相關活動的內容和要求。
人因設計確認若采用總結性可用性測試方式則提交總結性可用性測試計劃與報告��,若采用等效醫療器械對比評價方式則提交等效醫療器械對比評價報告��。相關報告具體內容詳見第五章��。
8.可追溯性分析
提交申報醫療器械的人因設計可追溯性分析報告����,即追溯用戶接口的需求、設計����、驗證與確認��、風險管理的關系表����。
若無單獨的人因設計可追溯性分析報告���,可提供產品設計可追溯性分析報告并注明人因設計可追溯性分析所在位置��。
9.結論
簡述申報醫療器械的人因設計過程和結果�,說明使用錯誤對于用戶的影響情況以及綜合剩余風險是否均已降至可接受水平�����,判定其用戶接口安全有效性是否滿足要求。
若使用現成用戶接口,在核心要素����、人因設計過程��、需求規范��、使用風險管理、驗證與確認、可追溯性分析中予以說明。
(二)使用錯誤評估報告
使用錯誤評估報告用于細化風險管理報告關于可用性方面的內容�����,僅適用于中�����、低使用風險醫療器械���,包括基本信息���、使用風險級別�、核心要素、使用風險管理����、同類醫療器械上市后使用問題分析�、結論等內容�,具體要求詳見上文人因設計研究報告、等效醫療器械對比評價報告相應條款說明�。
若使用現成用戶接口���,在核心要素���、使用風險管理����、同類醫療器械上市后使用問題分析中予以說明���。
八、注冊申報資料補充說明
(一)產品注冊
1.研究資料
對于高使用風險醫療器械��,在“CH3.8其他資料”中提交人因設計研究報告���。其中����,在驗證與確認部分,全新產品原則上提交總結性可用性測試報告,成熟產品可提交等效醫療器械對比評價報告��。
對于中、低使用風險醫療器械,在“CH3.2風險管理”中提交使用錯誤評估報告����。若前期已開展人因設計工作�,亦可在“CH3.8其他資料”中提交人因設計研究報告,用于替代相應使用錯誤評估報告。
相關研究資料具體要求詳見第七章�。若相應文檔在其他注冊申報資料中可予以引用���。
2.用戶培訓方案
對于高使用風險醫療器械�,原則上需在人因設計研究資料中提交用戶培訓方案,包括用戶培訓的計劃�、材料���、方式、師資�、效果評估等內容�����。
對于中、低使用風險醫療器械�,無需提交用戶培訓方案�。
3.說明書與標簽
說明書原則上需明確醫療器械的用戶/用戶組�����、用戶特征�����、用戶限制(如特殊人群用戶���、患有特定疾病或服用特定藥物的用戶)��、使用場所、環境條件����、操作任務���、人機交互方式等必要信息��,包括全部關鍵任務相關使用錯誤的安全信息����。
對于兼為緊急任務�����、常用任務的關鍵任務�,若通過標簽提供使用錯誤安全信息進行風險控制,則需提交相應標簽樣稿���。
(二)變更注冊
根據人因設計更改情況提交相應變化對產品安全性與有效性影響的研究資料。
對于高使用風險醫療器械���,在“CH3.8其他資料”中提交相應研究資料:用戶����、使用場景�、用戶接口發生實質性更改提交關于變化的人因設計研究報告,發生非實質性更改提交質量管理體系所形成的相應評估文檔�,未發生更改提交真實性聲明并明確對此承擔法律責任即可�。
對于中���、低使用風險醫療器械���,在“CH3.2風險管理”中提交相應研究資料:用戶���、使用場景�、用戶接口發生實質性更改提交關于變化的使用錯誤評估報告,其他情形與高使用風險醫療器械要求相同���。若前期已開展人因設計工作,亦可在“CH3.8其他資料”中提交關于變化的人因設計研究報告���,用于替代相應使用錯誤評估報告���。
若適用���,提交用戶培訓方案�、說明書與標簽的變化說明及其影響評估文檔。
(三)延續注冊
延續注冊通常無需提交人因設計研究資料����。若適用�,根據注冊證“備注”所載明的要求提交相應人因設計研究資料。
九、參考文獻
[1] 原國家食品藥品監督管理總局. 醫療器械說明書和標簽管理規定: 國家食品藥品監督管理總局令第6號[Z], 2014.7.
[2] 原國家食品藥品監督管理總局. 醫療器械召回管理辦法:國家食品藥品監督管理總局令第29號[Z], 2017.1.
[3] 國家市場監督管理總局. 醫療器械不良事件監測和再評價管理辦法: 國家市場監督管理總局令第1號[Z], 2018.8.
[4] 國家市場監督管理總局. 醫療器械注冊與備案管理辦法:國家市場監督管理總局令第47號[Z], 2021.8.
[5] 原國家食品藥品監督管理總局. 醫療器械生產質量管理規范: 國家食品藥品監督管理總局2014年第64號公告[Z], 2014.12.
[6] 國家藥品監督管理局. 醫療器械唯一標識系統規則: 國家藥品監督管理局2019年第66號公告[Z], 2019.8.
[7] 國家市場監督管理總局. 醫療器械注冊申報資料要求和批準證明文件格式: 國家市場監督管理總局2021年第121號公告[Z], 2021.9.
[8] 國家市場監督管理總局. 體外診斷試劑注冊申報資料要求和批準證明文件格式: 國家市場監督管理總局2021年第122號公告[Z], 2021.9.
[9] 國家藥品監督管理局. 醫療器械注冊自檢管理規定: 國家藥品監督管理局2021年第126號公告[Z], 2021.10.
[10] 國家藥品監督管理局. 醫療器械生產質量管理規范附錄獨立軟件: 國家藥品監督管理局2019年第43號通告[Z], 2019.7.
[11] 國家藥品監督管理局. 植入式左心室輔助系統注冊技術審查指導原則: 國家藥品監督管理局2020年第17號通告[Z], 2020.3.
[12] 國家藥品監督管理局. 醫療器械安全和性能的基本原則: 國家藥品監督管理局2020年第18號通告[Z], 2020.3.
[13] 國家藥品監督管理局. 醫療器械臨床評價技術指導原則: 國家藥品監督管理局2021年第73號通告[Z], 2021.9.
[14] 國家藥品監督管理局. 醫療器械生產質量管理規范獨立軟件現場檢查指導原則: 藥監綜械管〔2020〕57號[Z], 2020.5.
[15] 國家藥品監督管理局醫療器械技術審評中心. 家用醫療器械說明書注冊技術審查指導原則(征求意見稿)[Z], 2019.11.
[16] GB 9706.1-2020, 醫用電氣設備 第1部分:基本安全和基本性能的通用要求[S].
[17] YY/T 9706.106-2021, 醫用電氣設備 第1-6部分:基本安全和基本性能的通用要求 并列標準:可用性[S].
[18] YY 9706.108-2021, 醫用電氣設備 第1-8部分:基本安全和基本性能的通用要求 并列標準:通用要求�,醫用電氣設備和醫用電氣系統中報警系統的測試和指南[S].
[19] YY/T 9706.110-2021, 醫用電氣設備 第1-10部分:基本安全和基本性能的通用要求 并列標準:生理閉環控制器開發要求[S].
[20] YY 9706.111-2021, 醫用電氣設備 第1-11部分:基本安全和基本性能的通用要求 并列標準:在家庭護理環境中使用的醫用電氣設備和醫用電氣系統的要求[S].
[21] YY 9706.112-2021, 醫用電氣設備 第1-12部分:基本安全和基本性能的通用要求 并列標準:預期在緊急醫療服務環境中使用的醫用電氣設備和醫用電氣系統的要求[S].
[22] GB/T 5703-2010, 用于技術設計的人體測量基礎項目[S].
[23] GB 10000-1988, 中國成年人人體尺寸[S].
[24] GB/T 13547-1992, 工作空間人體尺寸[S].
[25] GB/T 18976-2003, 以人為中心的交互系統設計過程[S].
[26] GB/T 21051-2007, 人-系統交互工效學 支持以人為中心設計的可用性方法[S].
[27] GB/T 22187-2008, 建立人體測量數據庫的一般要求[S].
[28] GB/T 23700-2009, 人-系統交互人類工效學 以人為中心的生命周期過程描述[S].
[29] GB/T 23701-2009, 人-系統交互人類工效學 人-系統事宜的過程評估規范[S].
[30] GB/T 42061-2022, 醫療器械 質量管理體系 用于法規的要求[S].
[31] GB/T 42062-2022, 醫療器械 風險管理對醫療器械的應用[S].
[32] YY/T 0466.1-2016, 醫療器械 用于醫療器械標簽�����、標記和提供信息的符號 第1部分:通用要求[S].
[33] YY/T 0466.2-2015, 醫療器械 用于醫療器械標簽����、標記和提供信息的符號 第2部分:符號的制訂�、選擇和確認[S].
[34] YY/T 0910.1-2013, 醫用電氣設備 醫學影像顯示系統 第1部分:評價方法[S].
[35] YY/T 1474-2016, 醫療器械 可用性工程對醫療器械的應用[S].
[36] YY/T 1864-2022, 脊柱內固定系統及手術器械的人因設計要求與測評方法[S].
[37] YY/T 1630-2018, 醫療器械唯一標識基本要求[S].
[38] YY/T 1681-2019, 醫療器械唯一標識系統基礎術語[S].
[39] YY/T 1879-2022, 醫療器械唯一標識的創建和賦予[S].
[40] FDA. Guidance on Medical Device Patient Labeling[Z], 2001.4.
[41] FDA. Design Considerations for Devices Intended for Home Use[Z], 2014.11.
[42] FDA. Applying Human Factors and Usability Engineering to Medical Devices[Z], 2016.2.
[43]FDA. List of Highest Priority Devices for Human Factors Review (Draft Guidance)[Z], 2016.2.
[44] FDA. Content of Human Factors Information in Medical Device Marketing Submissions (Draft Guidance)[Z], 2022.12.
[45] FDA. Application of Human Factors Engineering Principles for Combination Products: Questions and Answers[Z], 2023.9.
[46] MHRA. Human Factors and Usability Engineering - Guidance for Medical Devices Including Drug-device Combination Products[Z], 2017.9.
[47] ANSI/AAMI HE75:2009/(R)2018, Human factors engin eering - Design of medical devices[S].
[48] IEC 62366-1:2015, Medical devices - Part 1: Application of usability engineering to medical devices[S].
[49] IEC/TR 62366-2:2016, Medical devices - Part 2: Guidance on the application of usability engineering to medical devices[S].
[50] Michael Wiklund, Jonathan Kendler, Allison Y. Strochlic [著]. 張強, 彭明辰[譯]. 醫療器械可用性測試[M], 人民衛生出版社, 2013.11.
[51] ISO/TC159 Ergonomics[OL]. https://www.iso.org/committ ee/53348.html.
[52] SAC/TC7全國人類工效學標準化技術委員會[OL].
標簽:可用性工程文檔編制服務